Reducción de cinética química
Uno de los motivos más importantes para el desarrollo de cinéticas reducidas es su incorporación en simulaciones de llamas turbulentas, donde el empleo de químicas detalladas puede hacer el problema intratable por el alto coste computacional asociado. Aunque recientemente el empleo de química tabulada (en modelos PDF) ha demostrado su potencial, el uso de química reducida sigue siendo una alternativa eficaz en cálculos LES y DNS. La química reducida es útil también en estudios analíticos de estabilidad y dinámica de llamas. Una de las líneas de investigación del Grupo es la reducción de la cinética química de hidrógeno y del gas sintético (mezclas H2/CO) basándose en la hipótesis de estado estacionario y equilibrio parcial.
Química reducida del hidrógeno
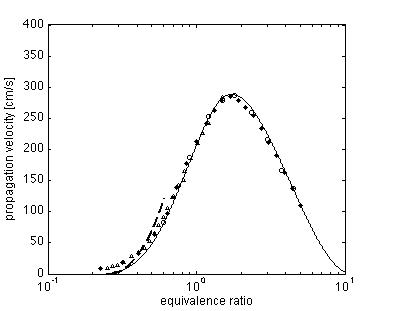
De las 21 reacciones elementales involucradas en la combustión del hidrógeno, a día de hoy sabemos que es posible la reducción a una química de un paso 2H2 + O2 ⇒ 2H2O para deflagraciones pobres de hidrógeno (Fernández-Galisteo et al. 2009) y a tres pasos 3H2 + O2 ⇔ 2H2O + 2H, H + H + M ⇔ H2 + M y H2 + O2 ⇔ HO2 + H para la descripción completa de llamas premezcladas, no premezcladas y autoignición (Boivin et al. 2011). La figura inferior muestra la velocidad de propagación de llamas de hidrógeno-aire en condiciones estándar en función del dosado. En la figura se muestran resultados de cálculos con química detallada que incorporan las 21 reacciones elementales de la oxidación del hidrógeno (línea continua), resultados de cálculos con cinética reducida de un paso (línea discontinua) y medidas experimentales de múltiples autores (símbolos).
En la figura inferior se muestra el campo instantáneo de temperaturas en una simulacion LES-DNS de una llama supersónica de hidrógeno-aire estabilizada por autoignición. A la izquierda los resultados empleando química detallada y a la derecha usando la química reducida de tres pasos. El próposito es comprobar que la química reducida describe correctamente la estructura de estas llamas incluso cuando los procesos de autoignición, difusión y premezclado se encuentran inmersos en flujos muy fluctuantes.


Química reducida del gas sintético (syngas)
La combustión del gas sintético para condiciones típicas de funcionamiento en turbinas de gas puede describirse mediante una química reducida de cuatro pasos (Boivin et al. 2011). El cuarto paso consiste en la oxidación del CO para dar CO2 a través de la reacción global CO + H2O ⇔ CO2 + H2 y con un ritmo de reacción que depende de dos reacciones elementales que involucran CO y especies intermedias como el H, OH y HO2. En ausencia de esta cuarta reacción la química se reduce a los tres pasos para la combustión del hidrógeno-aire. En la figura inferior se muestra la velocidad de propagación con el dosado a cuatro presiones distintas y para dos grados distintos de dilución en el ratio H2/CO. En la figura se muestran los resultados calculados con la química detallada de San Diego que involucra 30 reacciones elementales (líneas sólidas), con un esquema corto de 16 reacciones elementales (línea discontínua), y con el mecanismo reducido de cuatro pasos (líneas de trazos y puntos). Además, se muestran en símbolos el valor obtenido en ensayos experimentales

